Patologie > Carcinosi Peritoneale/Metastasi Peritoneali da Carcinoma Ovarico > Per saperne di piu’ su Metastasi Peritoneali da Carcinoma Ovarico
Per saperne di piu’ su Metastasi Peritoneali da Carcinoma Ovarico
I tumori epiteliali dell’ovaio rappresentano la seconda neoplasia più frequente dell’apparato genitale femminile, nonché la più letale tra quelle ginecologiche, con una sopravvivenza a 5 anni stimata del 39%.
Nonostante gli sforzi volti ad individuare un metodo di screening efficace per questa neoplasia, il 70% delle pazienti giunge alla diagnosi ad uno stadio avanzato (III - IV stadio FIGO) ovvero in presenza di metastasi peritoneali (MP)
La diagnosi di CA Ovarico avviene spesso in maniera accidentale, durante esami di controllo od interventi eseguiti per altra patologia. Infatti, la sintomatologia è tardiva, legata cioè alla diffusione intraperitoneale di malattia. Negli stadi finali, gran parte di questi casi sono caratterizzati da un quadro clinico ingravescente con presenza di ascite, aumento volumetrico dell’addome e del peso corporeo, dolori addominali diffusi con (sub)occlusione, difficoltà respiratorie o di alimentazione, astenia e cachessia.
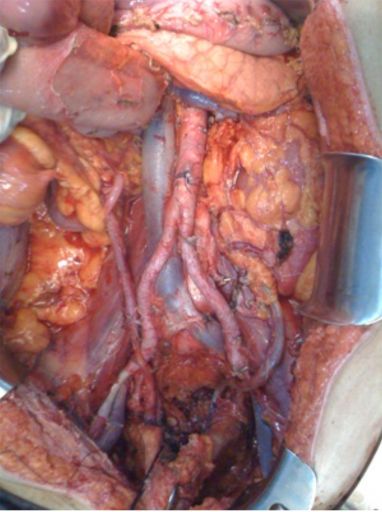
Il trattamento standard del Carcinoma Ovarico in presenza di MP consiste nell’associazione del trattamento chirurgico e della chemioterapia sistemica (sCT). Il trattamento chirurgico è stato tradizionalmente definito dai ginecologi “Chirurgia di Debulking” (isteroannessectomia bilaterale, omentectomia infracolica, biopsie linfonodali e peritoneali) se eseguito prima della sCT oppure “Interval Debulking” se eseguito dopo la sCT neoadiuvante. Effettivamente il termine significa asportare quanta più malattia possibile con accettazione dell’eventuale residuo di malattia. Tuttavia nel corso del tempo, grazie ad alcuni contributi scientifici tra cui quelli di Bristow, che hanno valutato gli effetti della chirurgia sulla sopravvivenza nel cancro ovarico avanzato, si è compreso che la radicalità chirurgica costituisce il fattore che influenza maggiormente la prognosi dei pazienti. Il termine debulking è stato pertanto sostituito con quello di Chirurgia Citoriduttiva (CRS) il cui obiettivo è quello di ottenere una radicalità chirurgica. Ovviamente nella CRS l’estensione dell’atto chirurgico è maggiore mediante procedure chirurgiche aggiuntive alla chirurgia standard (peritonectomia, resezione del diaframma, resezioni intestinali estese, splenectomia, gastrectomia parziale, resezioni epatiche, pancreatiche e resezioni renali, linfoadenectomia aortica) Fig 1.
Purtroppo è piuttosto scarsa la percentuale di pazienti con Ca Ovarico che ha accesso ad un trattamento corretto soprattutto chirurgico. Uno studio americano condotto da Robert Bristow ha stimato che solo il 37,2% delle pazienti americane riceve un trattamento in accordo con le linee guida NCCN (National Comprehensive Cancer Network). Ciò prevalentemente in quanto il trattamento chirurgico del Ca Ovarico necessita di capacità tecniche dei chirurghi elevate ed inoltre di personale specializzato per la corretta ed efficace conduzione anestesiologica e post-operatoria. Tali competenze sono evidentemente limitate solo ad alcuni centri di riferimento.
L’ordine con cui tali trattamenti vengono offerti dipende dall’estensione di malattia e dalla possibilità di ottenere una citoriduzione completa. Di fatto la sequenza di trattamento standard raccomandata dal NCCN consiste nella CRS seguita dalla sCT mentre la sequenza opposta si applica quando l’estensione di malattia non consente una chirurgia radicale oppure le condizioni generali della paziente sono tali da non consentire un atto chirurgico complesso. Tuttavia non vi sono studi randomizzati che confermino che una sequenza sia migliore dell’altra.
Nonostante il tumore ovarico sia tra le neoplasie solide più chemioresponsive e la sopravvivenza a 5 anni sia migliorata negli ultimi anni, circa il 60% delle donne svilupperà una recidiva. In queste, la sopravvivenza a lungo termine rimane modesta. Per questo motivo, sono stati proposti diversi approcci terapeutici più aggressivi, sia in prima linea sia sulla recidiva, come per esempio la citoriduzione secondaria, la chemioterapia intraperitoneale (IP) e la HIPEC.
La chemioterapia IP ha avuto un notevole impulso dopo la pubblicazione di almeno 3 studi prospettici randomizzati, che dimostravano come la somministrazione, dopo chirurgia ottimale, di agenti citotossici direttamente nella cavità peritoneale migliorava in maniera statisticamente significativa la prognosi delle pazienti affette da carcinoma ovarico avanzato. Tuttavia, questo tipo di procedura, non associata all’ipertermia e non in anestesia, era gravata da una certa percentuale di complicanze, prima tra tutte il dolore riferito dalle pazienti e l’infezione nel sito di inoculo, tanto da determinare un abbandono del trattamento nel 54% delle pazienti. Le ragioni del successo in termini prognostici sono facilmente individuabili nella possibilità di ottenere una più alta concentrazione dei farmaci a livello della malattia microscopica residua, senza però avere gli effetti di tossicità che si riscontrano invece nelle somministrazioni endovenose ad alte dosi. Infatti, i farmaci somministrati per via intraperitoneale possono agire direttamente sulla massa tumorale, bypassando l’ostacolo della scarsa vascolarizzazione nella malattia ed aumentando la concentrazione peri- ed intratumorale del farmaco stesso. Il Cisplatino può penetrare fino a 1-3 mm di profondità; ovviamente il beneficio per questa via di somministrazione è ottenibile solo in caso di residuo microscopico di malattia. Inoltre, una sufficiente quantità del farmaco passa comunque nel circolo sistemico, garantendo dunque un certo controllo anche sulla malattia a distanza.
Bisogna comunque ricordare che l’efficacia della chemioterapia IP è condizionata dall’omogenea distribuzione dei farmaci nella cavità. Nelle pazienti sottoposte a chirurgia citoriduttiva spesso si formano aderenze intraperitoneali che possono limitarla libera circolazione del farmaco. Pertanto, la IP intra-operatoria sembra una valida alternativa per superare questo limite. Inoltre, il trattamento in condizioni ipertermiche, aumentando la pervietà delle membrane cellulari, consente un’aumentata concentrazione dei farmaci all’interno dei tessuti e delle cellule tumorali.
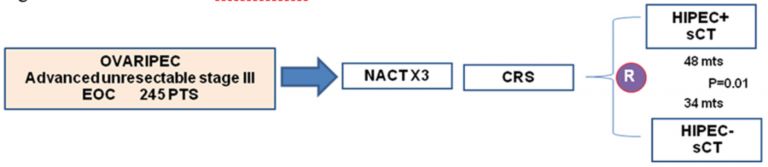
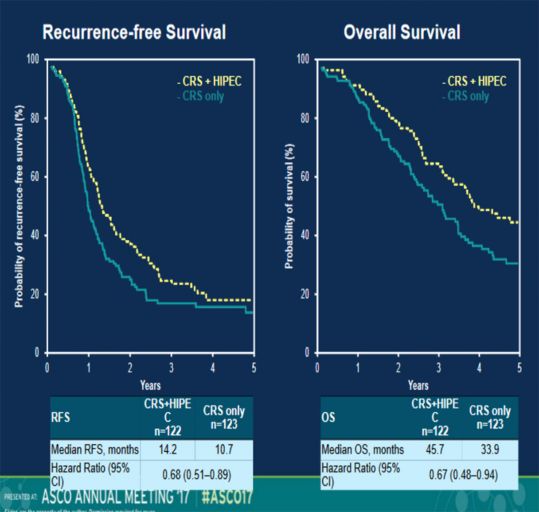
Il superamento di tali limiti sembra essere offerto dall’introduzione, nell’ambito di vari studi clinici, della HIPEC. La combinazione CRS e HIPEC rappresenta una potenziale opzione di trattamento. Numerosi sono gli studi, sia prospettici che retrospettivi, per valutare l’efficacia dell’approccio CCR e HIPEC nei tumori dell’ovaio in fase avanzata. Tutti hanno dimostrato un aumento della sopravvivenza globale e della sopravvivenza libera da malattia. Uno studio Fase II condotto in Italia ha evidenziato una sopravvivenza a 5 anni superiore a 60% quando i pazienti ricevevano un trattamento di CRS HIPEC con chirurgia estesa e completa in prima linea seguita da sCT. Una metanalisi condotta da un gruppo australiano ha consentito di dimostrare che l’associazione della HIPEC alla CRS e sCT consente il miglioramento di circa un anno di sopravvivenza delle pazienti. Un recente studio randomizzato presentato ad ASCO 2017 ha infine consentito di dimostrare che le pazienti a cui viene associata la HIPEC dimostrano una riduzione statisticamente significativa del rischio di recidiva. Tali risultati sono stati recentemente confermati da uno studio olandese, randomizzato, condotto su pazienti con Ca Ovarico avanzato trattati con sCT neoadiuvante seguita da CRS HIPEC vs CRS sola all’interval debulking. Vi è stato un significativo (p= 0.01) della sopravvivenza nel gruppo di pazienti 8122) trattati con CRS HIPEC (=48 mesi) rispetto al gruppo (=122) di pazienti trattati con la sola chirurgia (=34 mesi). Fig. 2-3.